从数据看:患者中心性与罕见病临床试验成功的潜力
全球孤儿药销量正在上升。要避免触达超罕见人群时可能遇到的陷阱,关键在于:绘制患者就医路径、降低试验负担,并与患者倡导组织开展合作。
作者:Jonathan Kornstein(罕见病与儿科副总裁)
在各国的公共卫生政策层面,罕见病通常被界定为仅影响极小人口比例的疾病;但从全球范围看,合计患者人数已超过3亿,并逐渐成为生物医药行业的重要增长领域。
受《孤儿药法案》等激励政策与遗传学进步推动,少见疾病的药物开发正在提速。根据 GlobalData 的预测,全球孤儿药销售额到2028年有望接近2750亿美元,年均增长约12%。大量生物医药企业加大投入;孤儿药在新药获批中的占比持续上升。
尽管前景可观,但面向数量稀少、地域分散的患者人群开展研发极具挑战性。80%的临床试验无法在既定时间内完成入组,且超过一半因患者纳入不足而被迫提前终止。孤儿药赛道虽快速扩张且具有吸引力,但对于研究者而言仍是风险高且复杂度大的领域。
入组与留存的挑战
阻碍罕见病临床试验成功的最大障碍是什么?毫无疑问,是入组与留存。符合条件的患者极少且分布分散,迫使即使是早期研究也不得不采用复杂的跨国多中心设计;而传统招募方式很难有效触达这类人群。一项近期分析显示,在罕见病试验中被筛查的患者有81%不符合入组条件——比非罕见病试验高出34个百分点——这反映出此类研究通常具有更严格的入排标准。研究团队往往需要从数十份转诊中筛出一名符合条件的患者。
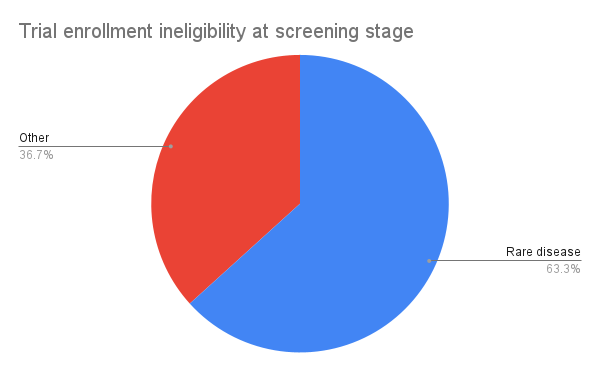
图1:筛查阶段的入组不符合比例——罕见病试验 vs. 非罕见病试验。Source: https://www.appliedclinicaltrialsonline.com/view/proliferation-rare-disease-rd-necessitating-novel-strategies.
这种“入组紧缩”对罕见病研究影响深远。除难以达到入组目标外,罕见病开发周期平均比非罕见病长约四年,主要原因在于临床机构与患者招募延迟。一项针对2010年代早期登记的659项罕见病试验的研究发现,超过一半的研究在四年内被终止或未发表,主要由于无法招满患者。GlobalData 的临床试验数据库进一步印证了这一点:在过去两年中被中止、终止或撤回的罕见病试验里,最常见的原因是“未指明”,这通常意味着试验甚至未能真正启动。
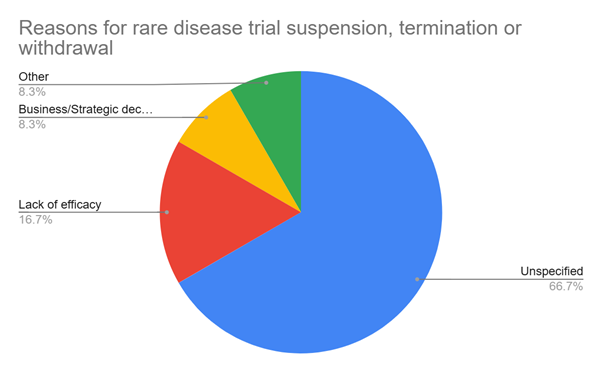
图2:罕见病试验被中止/终止/撤回的原因分布。“未指明”在此处通常意味着试验未能真正启动。Source: GlobalData.
留存同样关键。平均而言,约30%的受试者会在研究完成前退出。对于样本量常常只有几十人的罕见病试验而言,即便失去一两名受试者,也可能动摇结果的统计学效力。简言之,每一位患者都至关重要;让他们保持参与与获得支持,与最初的招募同等重要。
通过患者中心化设计降低负担
“以患者为中心”的试验设计——让研究围绕患者生活而非迫使患者适应研究——有望扭转上述局面。通过分析患者接受诊疗的地点、出行方式、所需支持与面临障碍,方案设计者可制定贴合患者日常而非颠覆其生活节奏的研究流程。一个具有变革性的趋势是:罕见病领域去中心化与混合式临床试验的崛起。去中心化要素包括远程医疗随访、上门护理、直达患者用药发放,以及各类居家、移动与可穿戴方式等——把研究带到患者身边。尽管其热度在解封后有所回落,但纳入去中心化方法的试验正获得实实在在的收益。除缩短时间线外,GlobalData 的数据还显示,这类试验的成功率高于总体平均。
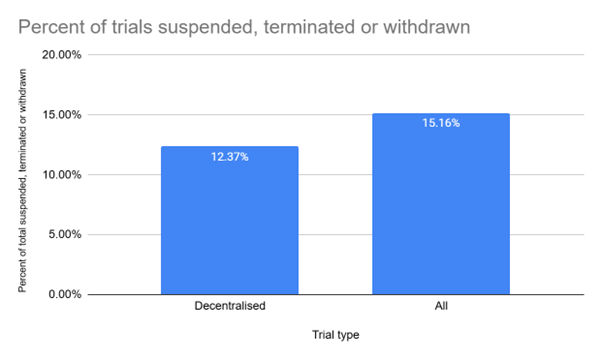
图3:按试验类型划分的中止/终止/撤回比例。去中心化试验的“暂停率”低近3个百分点。Source: GlobalData.
进一步剖析数据可见,罕见病研究者正以独特方式运用去中心化的潜在优势。
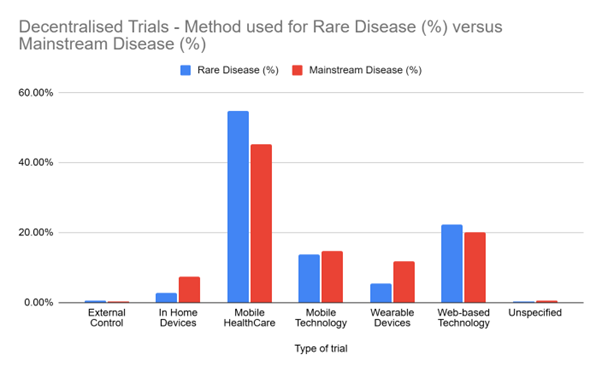
总体趋势一致——移动医疗是最常见的去中心化方式,“外部对照”最少;但罕见病与常见病之间也存在显著差异:例如,移动医疗在罕见病试验中的应用比例高出近10个百分点。此外,尽管绝对数较小,罕见病研究团队采用“外部对照”的可能性是常见病团队的两倍多。这凸显了触达难以覆盖人群所需的定制化技术路径,以及特定的去中心化要素如何帮助研究者实现这一点。
采用适应性试验设计、主方案或替代终点等策略,可在更少患者的前提下实现有意义的结果。实际上,根据 GlobalData 的数据库分析,与常见病相比,罕见病试验采用“适应性终点”的可能性约高出51%。监管机构也在鼓励新方法——从适应性剂量探索到历史对照——以提升小样本研究的可行性。在兼顾科学严谨与参与便利的前提下,这些举措可同时提升入组与留存。
借力患者倡导组织与全球化布局
要打造真正以患者中心的罕见病试验,尽早且深入地与患者倡导组织(PAGs)合作至关重要。罕见病PAGs多由患者及其家属发起,已成为试验设计与招募中的不可或缺伙伴。
这些组织通过社交媒体、患者登记与年度大会等方式维系强大的网络,可以连接地域分散的患者;一项最新研究显示,81%的罕见病倡导组织参与过临床研究,54%协助建立过患者登记库,16%甚至发起过自己的试验。
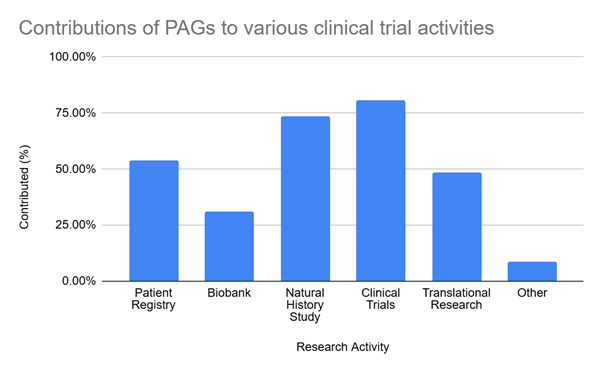
图5:近期调查中罕见病PAGs在各类研究活动中的贡献。超过80%参与过罕见病临床试验;另有16%实际发起了自身试验。Source: Young et al. (2023).
从一开始就与PAGs协作,申办方即可借助其网络提升试验知晓度,并对可能被忽略的潜在受试者进行预筛。同时,PAGs也能在方案筹划阶段成为“患者之声”:帮助确定患者真正关切的结局指标、现实可行的时间表/程序,以及如何与患者社区进行有效沟通。
通过以患者需求为中心的协作理念,可提升志愿参与试验的患者真正推动“治愈之路”的概率——同时避免患者与申办方彼此浪费时间。
有效的罕见病研究往往需要全球视野。国际多中心试验固然叠加了多重复杂性:多重监管框架、语言与文化差异,以及跨国转运样本或治疗的物流挑战;但这也是达到“临界样本量”的唯一途径。实践表明,申办方有时需要在数十个国家开设临床机构,才能招募到仅相当于常见病试验15%的志愿者数量。“到患者所在之处去”是罕见病研究成功的关键。瞄准尚未触达的区域(如新兴市场)可显著提升入组率。在一项FOP研究中,我们得以利用中国这一尚未触达的人群来源,显著增加入组并压缩整体时间线。与能够把研究者带到“必要地点”的PAGs合作,以及与能建立相应联系的专业伙伴协作,至关重要。
前路:以目标为导向的合作伙伴关系
要克服罕见病试验相互交织的多重挑战——稀少的患者、复杂的物流、不断演进的法规——药物研发团队愈发需要与具备全球基础设施及以患者为中心思维的合同研究组织(CRO)合作。在一个没有任何单一公司能够在每个国家都保持业务覆盖、在每个疾病领域都具备深度的时代,战略合作至关重要。
精通罕见病患者路径的CRO能够设计真正以患者为中心的研究,以更有效地招募并留住受试者;运营敏捷性与灵活性同样关键。经验丰富的合作伙伴深知:在罕见病试验中,计划常常需要快速调整——可能需要放宽入组标准、检测可能失败、患者可能需要个性化便利——因此能在监管范围内依据新信息快速转向尤为宝贵。与大型官僚化组织不同,敏捷型CRO能够快速决策,并在监管范围内实时调整与定制试验以确保项目按计划推进。
以康缔亚(Caidya)为例,我们提供针对申办方需求的个性化方案:为从单项试验到全流程合作的各类项目配置定制化团队与灵活的运营模型。与康缔亚合作的申办方可直接对接资深领导层,确保每一步都具备战略一致性与快速响应。通过在同一平台整合技术、PAGs与监管专业能力,合适的合作伙伴能够让后勤执行力与科学愿景相匹配,使研究者与生物医药创新者专注于他们最擅长的科学研究本身。
随着孤儿药板块向2700多亿美元规模迈进,患者与创新者的利害攸关不断提升。但行业正在从“为患者设计试验”转向“与患者共同设计试验”。证据显示,这一转变将带来更快的入组、更好的留存与更有意义的临床结局。工作仍任重道远:数千种罕见病仍无获批疗法,许多研究者仍面临令人望而却步的进入门槛。但通过倾听患者声音、在患者所在之处与其相遇,并构建支持性的全球合作网络,新的路径正在不断被开辟。
